Shaanxi BLOOM Tech Co., Ltd. є одним із найдосвідченіших виробників і постачальників ін’єкцій зиконотиду в Китаї. Ласкаво просимо до оптових оптових оптових високоякісних ін’єкцій зиконотиду, які продаються на нашому заводі. Хороший сервіс і доступні ціни.
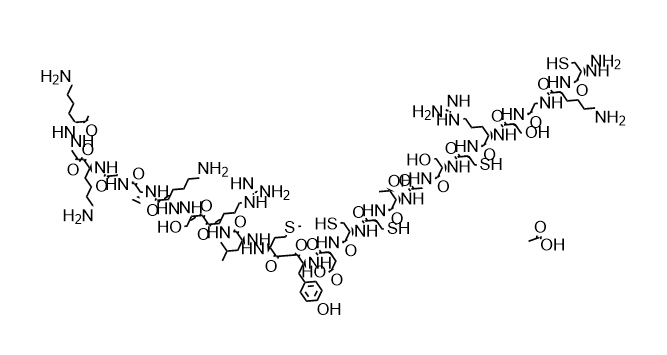
Діюча речовинаін'єкція зиконотидуце зиконотид, синтетичний ω-конотоксин, спочатку виділений і екстрагований з отрути морських конусних равликів і хімічно модифікований для отримання ін’єкційної форми. Він має молекулярну масу 2639,15 і номер CAS 107452-89-1. Механізм дії зіконотиду повністю відрізняється від механізму дії традиційних опіоїдів: замість дії на опіоїдні рецептори він надає аналгетичну дію шляхом вибіркової блокади кальцієвих каналів N-типу в центральній нервовій системі.
Форма для наших продуктів






Зиконотид поліацетат COA
 |
||
| Сертифікат аналізу | ||
| Складена назва | Зиконотид поліацетат | |
| Оцінка | Фармацевтичний клас | |
| Номер CAS | 107452-89-1 | |
| Кількість | 30g | |
| Упаковка стандартна | PE мішок + мішок з алюмінієвої фольги | |
| Виробник | Shaanxi BLOOM TECH Co., Ltd | |
| Лот № | 202601090088 | |
| MFG | 9 січня 2026 р | |
| EXP | 8 січня 2029 р | |
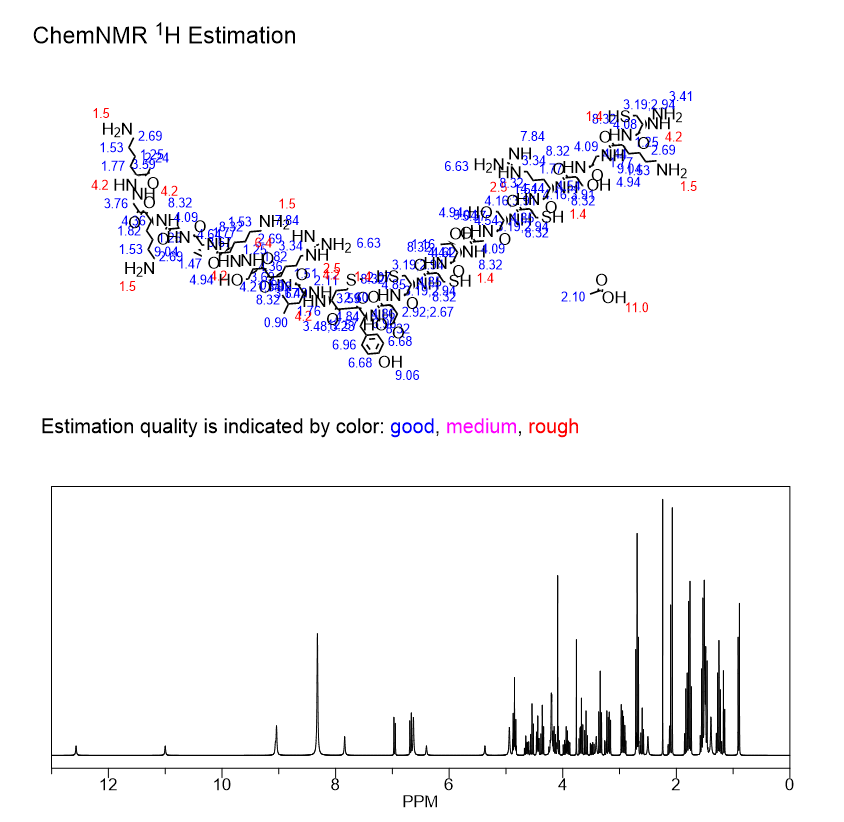
| Структура |
|
|
| Пункт | Стандарт підприємства | Результат аналізу |
| Зовнішній вигляд | Білий або майже білий порошок | Відповідає |
| Вміст води | Менше або дорівнює 5,0% | 0.54% |
| Втрати при висиханні | Менше або дорівнює 1,0% | 0.42% |
| Важкі метали | Pb Менше або дорівнює 0,5 ppm | N.D. |
| Менше або дорівнює 0,5 ppm | N.D. | |
| Hg Менше або дорівнює 0,5 ppm | N.D. | |
| Cd Менше або дорівнює 0,5 ppm | N.D. | |
| Чистота (ВЕРХ) | Більше або дорівнює 99,0% | 99.98% |
| Поодинока домішка | <0.8% | 0.52% |
| Загальне мікробне число | Менше або дорівнює 750 КУО/г | 95 |
| E. Coli | Менше або дорівнює 2 MPN/г | N.D. |
| Сальмонела | N.D. | N.D. |
| Етанол (за GC) | Менше або дорівнює 5000 ppm | 500 ppm |
| Зберігання | Зберігати в закритому, темному та сухому місці при температурі -20 градусів | |
|
|
||
|
|
||
| Хімічна формула: | C97H170N34O30S5 |
| Точна маса: | 2511 |
| Молекулярна маса: | 2513 |
| m/z: | 2511 (100.0%), 2513 (95.3%), 2511 (40.8%), 2513 (22.6%),2511 (21.5%), 2454 (17.2%), 2453 (12.6%), 2452 (12.0%), 2455 (11.7%), 2453 (11.2%), 2454 (6.5%), 2454 (6.2%), 2453 (5.9%), 2455 (4.5%), 2453 (4.0%), 2456 (3.9%), 2452 (3.8%), 2455 (2.8%), 2454 (2.7%), 2455 (2.5%), 2456 (2.0%), 2453 (2.0%), 2455 (1.9%), 2452 (1.9%), 2454 (1.6%), 2456 (1.5%), 2455 (1.4%), 2456 (1.4%), 2455 (1.3%), 2453 (1.1%), 2452 (1.1%), 2456 (1.1%), 2457 (1.0%) |
| Елементний аналіз: | C, 47.50; H, 6.99; N, 19.42; O, 19.57; S, 6.54 |

Раковий біль є одним із найпоширеніших симптомів у пацієнтів із пізньою стадією раку, що серйозно погіршує якість життя пацієнтів, прихильність до лікування та виживання. Як новий неопіоїдний анальгетик,Ін'єкція зиконотидудемонструє значні переваги в лікуванні резистентного ракового болю завдяки своєму унікальному механізму дії, певній аналгетичній ефективності та низькому потенціалу зловживання, слугуючи важливим доповненням до клінічної анальгетичної терапії.
Значення застосування при рефрактерному болі при раку

(I) Чітка цільова популяція та висока специфічність
Продукт показаний пацієнтам із рефрактерним раковим болем, у яких біль не контролюється належним чином (візуальна аналогова шкала, VAS більше або дорівнює 5), незважаючи на стандартизовану опіоїдну терапію, або які не можуть переносити побічні реакції, пов’язані з опіоїдами (наприклад, важке пригнічення дихання, важкий запор, сильна нудота та блювання). Він особливо підходить для пацієнтів із супутнім нейропатичним раковим болем, на який припадає понад 50% випадків рефрактерного ракового болю. Нейропатичний раковий біль має складний патогенез, головним чином спричинений інвазією нервів пухлиною, ушкодженням нерва внаслідок хіміотерапії або променевої терапії, і проявляється як пекучий, колючий або подібний до удару електричним струмом біль із низькою чутливістю до традиційні опіоїди.
Продукт забезпечує помітне знеболювання при цьому типі болю. Клінічні дослідження показують, що його інтратекальне вливання ефективно зменшує показники болю та покращує сон і якість життя у пацієнтів із резистентним раковим болем, які є толерантними до опіоїдів або не реагують на опіоїди. Серія випадків із 8 пацієнтів із рефрактерним раковим болем (5 із супутнім нейропатичним болем) повідомила, що всі пацієнти досягли значного зменшення болю протягом Через 3–5 днів після інтратекального введення зиконотиду в комбінації з морфіном. Один пацієнт, який не відповів на фентаніл, все ж досяг задовільного контролю болю після відновлення терапії зиконотидом, що підтверджує його цінність для пацієнтів, які не реагують на опіоїди.


(II) Значна анальгетична ефективність і властивості, що не викликають звикання
Знеболювальна сила його порівнянна з дією морфіну і навіть перевершує її у деяких пацієнтів із дозозалежним знеболюючим ефектом; Оптимального знеболення можна досягти шляхом повільного титрування дози. Численні клінічні дослідження підтверджують, що його інтратекальне вливання знижує показники болю більш ніж на 30% у пацієнтів із стійким до раку болем, причому у деяких людей рівень полегшення болю перевищує 70%. У рандомізованому, подвійному сліпому, плацебо-контрольованому клінічному дослідженні за участю 169 пацієнтів із сильним хронічним болем (включаючи пацієнтів із стійким болем при раку) лікування зиконотидом знизило середній бал за шкалою VAS на 31,2% порівняно з лише 6,0% у групі плацебо, що представляє статистично значущу різницю (P менше або дорівнює 0,001).
Порівняно з опіоїдами, найбільш помітна перевагаін'єкція зиконотидуце відсутність у нього потенціалу залежності. Він не діє на опіоїдні рецептори, не викликає фізичної чи психологічної залежності та не викликає симптомів абстиненції, що дозволяє безпечне тривале застосування. Ця функція особливо важлива для пацієнтів із прогресуючим раком, які потребують тривалої аналгезії, оскільки вона дозволяє уникнути додаткових страждань і тягаря лікування, пов’язаного з наркоманією. Крім того, препарат не викликає пригнічення дихання, забезпечуючи вищий профіль безпеки для пацієнтів з рефрактерним болем при раку та одночасною дихальною недостатністю, без ризику дихальної недостатності, спричиненої ліками.
(III) Синергічна комбінація з іншими анальгетиками для покращення терапевтичних результатів
У клінічному лікуванні резистентного ракового болю монотерапія часто не досягає ідеального знеболення, що робить комбіновану терапію звичайною стратегією. Продукт можна використовувати в поєднанні з опіоїдами, місцевими анестетиками (наприклад, бупівакаїном) та іншими анальгетиками для отримання синергічної аналгезії, зниження індивідуальних доз препарату та зниження частоти побічних реакцій.
Клінічні дослідження демонструють, що низькі дози зиконотиду в поєднанні з інтратекальним морфіном швидко контролюють стійкий до опіоїдів раковий біль, одночасно зменшуючи дозу морфіну та пов’язані з ним побічні реакції, такі як запор і пригнічення дихання. Серія випадків із 8 пацієнтів із рефрактерним болем при раку повідомила, що у всіх пацієнтів попередня інтратекальна терапія морфіном і бупівакаїном була невдалою, але досягнуто ефективного контролю болю після додаткової терапії зіконотидом, розпочатої з 0,5–1,0 мкг/день і титрованої в бік збільшення на 0,5 мкг кожні 4–7 днів (максимальна доза менше або дорівнює 10 мкг/день). Також було зменшено дозування морфіну, що підтвердило ефективність і безпеку комбінованої терапії.
Джерело інформації: інтратекальний зиконотид і морфін для знеболювання: серія випадків із восьми пацієнтів із стійким болем при раку, включаючи п’ять випадків невропатичного болю; Інтратекальний зиконотид у лікуванні хронічного незлоякісного болю: рандомізоване, подвійне сліпе, плацебо-контрольоване клінічне дослідження.

Хід клінічних досліджень і перспективи застосування

(I) Прогрес клінічних досліджень
За останні роки проведено численні вітчизняні та міжнародні клінічні дослідженняін'єкція зиконотидудля рефрактерного ракового болю, додатково підтверджуючи його анальгетичну ефективність і безпеку. Багатоцентрове, рандомізоване, подвійне сліпе, плацебо-контрольоване дослідження включало 457 пацієнтів із сильним хронічним болем (включаючи стійкий біль при раку), рандомізованих для прийому зиконотиду (268 пацієнтів) або плацебо (189 пацієнтів) з повільним титруванням дози протягом 21 дня.
Група зиконотиду показала зниження середнього показника болю на 12%, порівняно з 5% у групі плацебо (статистично значуще), з помітно меншою частотою побічних реакцій, ніж при швидкому титруванні. Реальні дані також підтверджують його клінічне використання. 18-місячне проспективне багатоцентрове обсерваційне дослідження (PRIZM Registry) включало 93 пацієнтів із сильним хронічним болем, які отримували інтратекальний зиконотид. Оцінка за допомогою числової шкали оцінки болю (NPRS) виявила значне зменшення болю через 12 тижнів і сприятливу довгострокову безпеку, що підтверджує його цінність для тривалої аналгезії.


Крім того, дослідження невропатичного болю при раку показують, що зиконотид забезпечує краще полегшення порівняно з традиційними опіоїдами, пропонуючи більш ефективний варіант для цієї групи пацієнтів.
Поточні клінічні дослідження вивчають оптимізовані режими дозування, включаючи стратегії комбінування та індивідуальне титрування дози, для подальшого покращення аналгезії та мінімізації побічних реакцій. Також проводяться дослідження в особливих популяціях (наприклад, пацієнти похилого віку, пацієнти з порушенням функції печінки або нирок) для підтримки індивідуальної клінічної терапії.
(II) Перспективи застосування
У зв’язку зі зростанням попиту на рефрактерне лікування болю при раку, цей продукт, як новий неопіоїдний анальгетик, має широкі клінічні перспективи. З одного боку, його унікальний механізм робить його життєво важливим терапевтичним варіантом для пацієнтів із толерантністю до опіоїдів або відсутністю відповіді, заповнюючи клінічну прогалину та покращуючи якість життя. З іншого боку, його властивості, що не викликають звикання та не пригнічують дихання, зменшують побічні ефекти та ризики лікування, особливо для пацієнтів із дихальною недостатністю або високим ризиком залежності. У міру розвитку клінічних досліджень його, ймовірно, буде додатково підтверджено для конкретних підтипів рефрактерного ракового болю з оптимізованими схемами та розширеними показаннями.

Тим часом ширше впровадження та стандартизація інтратекальної доставки ліків збільшить їх клінічне використання, що принесе користь більшій кількості пацієнтів. Розробка препаратів тривалої дії також буде напрямком майбутніх досліджень, спрямованих на зменшення частоти дозування та покращення зручності для пацієнтів і дотримання режиму лікування.
Слід зазначити, що він має поточні клінічні обмеження, включаючи відносно складний шлях введення (вимагає інтратекальної інфузії), високу частоту побічних реакцій і високу вартість, які обмежують його широке використання. Майбутні інновації в технологіях і контролі над витратами допоможуть усунути ці бар’єри, покращити клінічну доступність і принести користь більшій кількості пацієнтів з рефрактерним раковим болем.
Джерело інформації: інтратекальний зиконотид і морфін для знеболювання: серія випадків із восьми пацієнтів із стійким болем при раку, включаючи п’ять випадків невропатичного болю; Інтратекальний зиконотид у лікуванні хронічного незлоякісного болю: рандомізоване, подвійне сліпе, плацебо-контрольоване клінічне дослідження.
Додаткова гіперчутливість і протипоказання
Гіперчутливість Протипоказання: Протипоказаний пацієнтам із відомою гіперчутливістю до зиконотиду або будь-яких допоміжних речовин (оцтова кислота, стерильна вода для ін’єкцій тощо).
Протипоказання для інтратекального введення: Протипоказаний пацієнтам з інфекціями в місці інфузії, коагулопатією, обструкцією спинномозкового каналу або іншими розладами, що порушують циркуляцію спинномозкової рідини.
Джерело інформації: FDA Prescribing Information, DailyMed Database
FAQ
Чи зиконотид сильніший за морфін?
+
-
Фармакодинамічні дослідження на людині. У широкому діапазоні моделей тваринного болю інтратекальний зиконотид спричиняв потужні антиноцицептивні ефекти, які булипринаймні в десять разів сильніше, ніж інтратекальний морфін.
Для чого використовується зиконотид?
+
-
Зиконотид – інтратекальний анальгетик, який використовується для лікуванняхронічний біль. Інтратекальна терапія була введена в 1980-х роках як засіб лікування хронічного рефрактерного болю. Ліки, які найчастіше використовуються сьогодні, включають опіоїдні анальгетики, такі як морфін, і місцеві анестетики, такі як бупівакаїн.
Чи є зиконотид пептидом?
+
-
Зиконотид є пептидомз послідовністю амінокислот H-Cys-Lys-Gly-Lys-Gly-Ala-Lys-Cys-Ser-Arg-Leu-Met-Tyr{{13 }}Asp-Cys-Cys-Thr-Gly-Ser-Cys-Arg-Ser-Gly-Lys-Cys-NH2(CKGKGAKCSRLMYDCCTGSCRSGKC-NH2) і містить 3 дисульфідні зв’язки (Cys1-Cys16, Cys8-Cys20 і Cys15-Cys25).
Популярні Мітки: зиконотид ін'єкції постачальники виробники фабрика оптом купити ціна гуртом продам